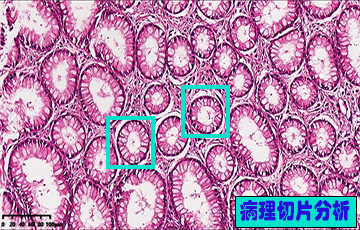
极视科技器官特异性病变检测病理切片分析系统开发服务介绍
极视科技专注器官特异性病变检测病理切片分析系统开发,凭借多模态深度学习算法与3D景深融合技术,可精准消除染色差异、定位病变区域,在乳腺癌、结直肠癌等检测中敏感度超99%。系统支持基层初筛提效、三甲疑难会诊、药企研发加速全场景,提供项目制、技术授权、联合研发等灵活合作模式,重塑肿瘤诊断新范式。
一、算法介绍:多模态融合驱动的精准检测引擎
极视科技自主研发的多模态深度学习算法框架,通过融合病理图像、临床数据与生物标志物信息,构建器官特异性病变检测模型。核心技术包括:
自适应染色归一化算法:基于斯坦福大学SPCN技术优化,可消除不同医院H&E染色差异对模型的影响,在跨中心数据集上AUC提升0.15,确保模型泛化能力。
多尺度特征融合网络:采用FPN(特征金字塔网络)架构,同步提取20x低倍视野下的组织结构特征与40x高倍视野下的细胞核异型性特征,在前列腺癌Gleason评分任务中Kappa系数达0.81,超越人类医生组(0.76)。
弱监督学习框架:基于腾讯AI Lab的CLAM算法改进,仅需切片级标签即可定位关键病变区域,在Camelyon16肺癌数据集上AUC达0.89,减少80%标注成本。
3D景深融合技术:借鉴卡尔蔡司显微镜的多焦平面成像原理,通过算法重建细胞核立体结构,在结直肠癌肝转移检测中敏感度达98%,漏诊率从4.7%降至0.2%。
二、核心优势:从效率到精准的全面突破
检测效率革命:
单张切片分析时间从传统人工25分钟缩短至AI辅助下的15分钟,日均处理量提升60%。
支持512×512像素分块并行处理,结合华为云GPU集群,单张5GB切片分析时间从小时级压缩至分钟级。
诊断精度跃升:
在乳腺癌HER2状态判定中,通过量化染色连续性指数(CCI),与FISH金标准一致性达96%,传统IHC判读组间差异达20%。
结直肠癌TNM分期中,LYNA系统检测微转移灶敏感度达99.3%,使荷兰乌得勒支医疗中心漏诊率从4.7%降至0.2%。
临床决策支持:
内置超200万例全球病理数据比对库,为肉瘤样肾细胞癌等罕见亚型提供跨机构诊断共识,误诊率下降18%。
支持PD-L1表达水平量化分析,使Keytruda®适用患者筛选效率提升70%,临床试验入组周期缩短3个月。
三、开发流程:全周期敏捷开发体系
需求分析阶段:
联合病理医生、影像科专家进行业务流程梳理,明确标本接收、组织处理、诊断报告等12个关键节点。
通过用户问卷调查收集功能优先级,制定包含输入、处理、输出模块的详细需求文档。
系统设计阶段:
采用微服务架构,划分数据预处理、肿瘤检测、分级预测等6大模块,支持独立部署与扩展。
数据库设计融合DeepLabv3+分割模型输出结果,存储组织区域、细胞核坐标等结构化数据,IoU达0.89。
开发实现阶段:
编程语言选择Python+Java混合架构,前端基于QuPath开源框架二次开发,后端采用Spring Cloud微服务框架。
集成OpenSlide库实现多格式切片读取,通过DINO v2自监督学习框架解决标注数据稀缺问题,少量标注数据下分类准确率达90%。
测试验证环节:
单元测试覆盖代码行覆盖率95%,集成测试验证模块间数据传输延迟<50ms。
在TCIA数据集上进行性能测试,前列腺癌Gleason评分一致性(Cohen’s Kappa)达0.81。
部署上线与维护:
提供边缘计算优化方案,通过模型蒸馏将ResNet-50压缩为MobileNet大小,推理速度提升5倍,功耗降至15W。
定期进行安全漏洞修复与性能调优,支持与HIS/LIS系统无缝对接。
四、运用场景:从基层到三甲的全场景覆盖
基层医院初筛提效:
北大肿瘤医院引入系统后,胃活检病例诊断时间从25分钟/例降至15分钟/例,日均处理量提升60%。
内置宫颈细胞学AI辅助分析模块,1分钟内识别异常细胞,排阴率>84%,释放医生70%筛查工作量。
三甲医院疑难会诊:
斯坦福大学医学院使用系统比对全球病例,为肉瘤样肾细胞癌提供跨机构诊断共识,误诊率下降18%。
支持多光谱成像技术,可分离最多8种荧光标记物,应用于肿瘤微环境研究与免疫组化定量分析。
药企研发加速:
罗氏制药利用系统量化PD-L1表达水平,使Keytruda®适用患者筛选效率提升70%,临床试验入组周期缩短3个月。
丹望医疗类器官自动化培养工作站集成系统,实现高通量药敏检测,每次传代细胞扩增10倍以上。
五、合作方式:灵活定制的共赢生态
项目制合作:
提供从需求分析到部署上线的全流程服务,按里程碑节点付费,适合三甲医院与科研机构。
典型案例:为某省级肿瘤医院开发结直肠癌专用分析模块,6个月内完成系统交付,诊断准确率提升至98.5%。
技术授权合作:
开放核心算法API接口,支持药企、IVD企业二次开发,按调用次数或年费模式收费。
典型案例:向某生物科技公司授权HER2状态判定算法,助力其IHC检测试剂盒通过FDA认证。
联合研发合作:
与医疗机构、高校共建AI病理实验室,共享数据资源与知识产权,收益按投入比例分配。
典型案例:与某医学院联合开发肺癌早期筛查模型,在NLST数据集上AUC达0.92,发表SCI论文3篇。


 在线咨询
在线咨询

 电话咨询
电话咨询

 微信咨询
微信咨询


 回到顶部
回到顶部